研究人员减少了亨廷顿氏干细胞模型的神经变性
CECAD的神经科学家David Vilchez博士及其团队是科隆大学衰老研究卓越集群,已朝着理解引起神经退行性疾病亨廷顿氏病的机制迈出了重要的一步。特别是,他们确定了一个阻止毒素蛋白聚集体积累的系统,该系统负责神经变性。结果现已发表在《自然通讯》杂志上。
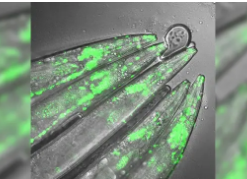
亨廷顿舞蹈病是一种神经退行性疾病,可导致脑细胞死亡,导致身体不受控制的运动,语言丧失和精神病。亨廷顿蛋白基因中的突变引起该疾病,导致亨廷顿蛋白的毒性聚集。这些聚集体的积累引起神经退行性变,通常导致疾病发作后二十年之内死亡。
为了检查亨廷顿氏病的潜在机制,Vilchez和他的团队使用了来自亨廷顿氏病患者的所谓诱导多能干细胞(iPSC),它们能够分化为任何细胞类型,例如神经元。来自亨廷顿氏病患者的诱导多能干细胞表现出惊人的能力,可以避免有毒蛋白质聚集体的积累,这是该疾病的标志。即使iPSC表达负责亨廷顿氏病的突变基因,也未发现任何聚集体。
研究人员确定了一种称为UBR5的蛋白质作为细胞的保护机制,从而促进了突变型亨廷顿蛋白的降解。这些发现可有助于更好地了解亨廷顿舞蹈病,并可为进一步开发患者治疗方法打下基础。
研究人员从患者和衍生的神经元中筛选了永生的iPSC,以了解它们避免突变的亨廷顿蛋白聚集能力的差异。他们发现亨廷顿蛋白可以被称为蛋白酶体的细胞处理系统降解。然而,该系统在神经元中是有缺陷的,这导致突变的亨廷顿蛋白异常聚集。Vilchez和他的团队发现,UBR5在多能干细胞中增加,从而加速了亨廷顿蛋白在细胞中的降解。为了检查UBR5在亨廷顿蛋白突变基因(HTT)调控中的作用,他们降低了UBR5的水平,并可以立即看到iPSC中聚集蛋白的积累。维尔切斯说:“这真是令人惊讶。”“从零开始,细胞变成了大量的聚集体。”
作者更进一步,研究了UBR5是否在亨廷顿氏病生物模型中也控制突变型亨廷顿蛋白聚集。实际上,他们发现UBR5失调导致神经元聚集和神经毒性作用大量增加。另一方面,促进UBR5活性可阻止亨廷顿氏病模型中的突变型亨廷顿蛋白聚集。
为了检验结果的特异性,研究人员还密切关注其他疾病。Vilchez实验室的博士生,刊物的主要作者Seda Koyuncu说:“我们还检查了肌萎缩侧索硬化症等其他神经退行性疾病的机制”。CECAD的另一位主要作者,伊莎贝尔·塞兹(Isabel Saez)博士补充说:“我们的结果对亨廷顿舞蹈症非常特定。”尽管结果对于治疗和药物开发可能很重要,但尚无治疗方法。塞兹评论说:“这不像您发现新的东西,然后找到治愈的方法,要困难得多,但是在某些年中可能会有一种治疗方法”。在此之前,还需要做更多的研究。
