艰难梭菌生物学的发现为开发用于危险感染的治疗方法打开
西奈山伊坎医学院的研究人员报告说,一种叫做孢子形成的过程可以帮助危险细菌艰难梭菌(C. difficile)在恶劣的条件下生存并传播,这种过程受表观遗传学的影响。这是表观遗传学调节任何细菌中孢子形成的第一个发现。他们的研究于11月25日发表在《自然微生物学》上,为开发这种毁灭性感染的治疗方法打开了一个新窗口。
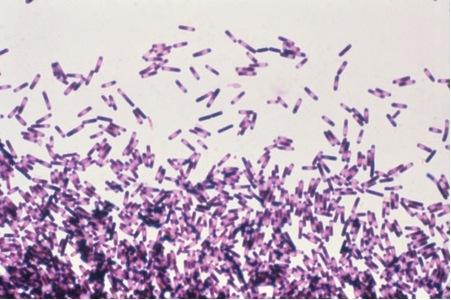
艰难梭菌每年感染近半百万人,引起严重腹泻,并杀死了65岁以上感染该病的人不到10%。细菌的孢子通过粪便传播,具有极强的韧性,可以在体外存活数周或数月,从而感染接触受污染表面的人。
由于这种感染非常普遍且具有毁灭性,因此艰难梭菌基因组已经得到了很好的研究,但是冈奈特博士(Gang Fang)博士,西奈山伊坎数据科学与基因组技术研究所遗传与基因组科学副教授,该研究的资深作者,他说,他和他的同事在研究中采用了不同的方法。Fang博士说:“我们想研究细菌的遗传密码,并研究对基因组进行了哪些化学修饰。”尽管这些称为甲基化的表观遗传化学修饰不会改变基因的序列,但它们可以修饰特定基因的活性以使其具有或多或少的活性,这对生物体的功能产生了深远的影响。
方博士的团队于2012年率先使用第三代DNA测序技术绘制了细菌中的表观遗传因子,并于2015年开始研究艰难梭菌的表观遗传学。首先,该团队从重症监护病房36名患者的粪便样本中分离了艰难梭菌。被感染的西奈山医院(ICU)。他们分析了样本,发现了一种特殊的表观遗传模式,在所有样本中其高度保守。接下来,他们检查了来自GenBank的大约300个艰难梭菌基因组,GenBank是由美国国立卫生研究院(National Institutes of Health)管理的遗传序列数据库,发现它们都共享相同的基因,该基因负责ICU患者的表观遗传模式。
方博士的团队怀疑这种表观遗传模式在细菌的功能中起着至关重要的作用,他们与艰难梭菌孢子形成和感染艰难梭菌的小鼠进行了两项进一步研究,由沉怡生博士实验室副研究员塔夫茨大学医学院的分子生物学和微生物学,也是该研究的共同作者,与北卡罗来纳大学教堂山分校微生物学和免疫学副教授Rita Tamayo博士一起使用。在一项关于小鼠的研究中,研究人员发现,当它们抑制负责表观遗传模式的基因时,与未改变的细菌相比,在6天后存在的细菌减少了多达100倍。
方博士说,这些研究的结果强调了表观遗传学在细菌和药物研发中的重要性。
方博士除了为艰难梭菌的研究提供新的表观遗传学见解以及可能的药物开发靶标外,还希望这项研究能够鼓励对细菌的表观遗传学特性进行进一步的研究。
