一种新的CRISPR-Cas9蛋白可提高基因编辑的精度
CRISPR(聚簇有规律间隔的短回文重复序列)-Cas9是一种有前途的基因编辑技术,从治愈许多遗传病到发展耐旱作物,其应用范围很广。使用CRISPR-Cas9治疗癌症,血液疾病和眼疾的临床试验正在进行中。
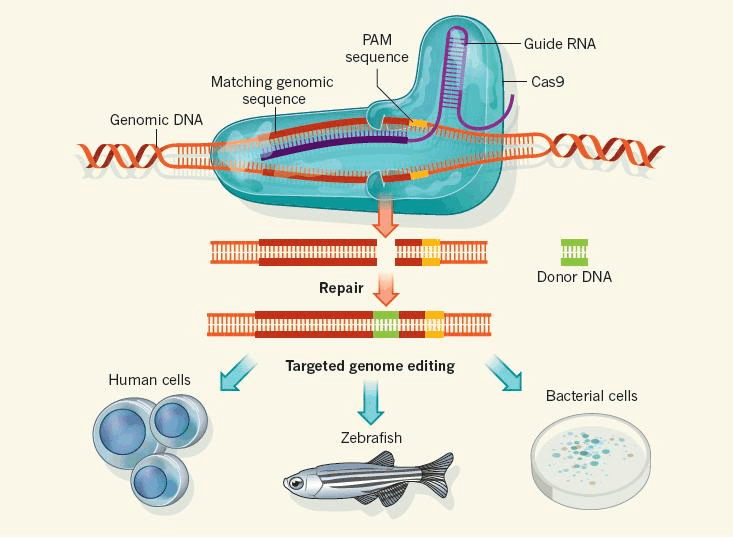
现场修复遗传缺陷
CRISPR-Cas9被认为是基因编辑的有力工具,因为它使基因修饰或编辑非常简单。与传统基因疗法不同,传统基因疗法将正常基因的其他副本引入细胞,CRISPR-Cas9通过去除有问题的DNA或对其进行纠正以恢复正常的基因功能来“修复”缺陷。
在此过程中,Cas9酶负责在进行修饰之前在整个基因组中定位有问题的DNA。但是发现有时它可能不够精确,并且可能发生基因组意外位置的DNA修饰。基因组的意外修改可能会导致严重后果,例如癌症,就像几年前在最初的基因治疗试验中所发生的那样。因此,重要的是让CRISPR-Cas9精确地对基因组进行“分子手术”。
目前,Cas9有两种版本,即SpCas9(意为化脓性链球菌的Cas9核酸酶)和SaCas9(意为金黄色葡萄球菌的Cas9核酸酶),它们通常在CRISPR中使用。它们都具有一定程度的不精确性或脱靶效应。研究人员已经设计出SpCas9变体,即经过修改的SpCas9,以提高SpCas9的定位精度。但是它可能太大而无法装入通常用于体内基因治疗的称为腺相关病毒(AAV)载体的小型传递载体中。
相反,SaCas9比SpCas9小得多,可以轻松地包装在有效载荷受限的AAV载体中,以在体内递送基因编辑成分。但是,没有具有高全基因组靶向准确性的SaCas9变体。
SaCas9-HF大大提高了全基因组靶向精度
由城大生物医学科学系助理教授郑宗礼博士及香港卡罗琳斯卡医学院明慧楼修复医学中心领导的最新研究,以及城大生物医学科学系助理教授史家海博士领导的研究,该团队已经成功设计了一种SaCas9-HF,这是一种CRISPR Cas9变体,在人类细胞全基因组靶向中具有很高的准确性,而不会影响靶向效率。
该研究小组的发现基于对24个目标人类遗传位置的严格评估,将原始未经修饰的(野生型)SaCas9与新的SaCas9-HF进行了比较。对于那些在基因组中具有高度相似序列并因此易于被野生型酶进行脱靶编辑的靶标,SaCas9-HF将脱靶活性降低了约90%。对于许多野生型酶的脱靶编辑相对较少的靶标,SaCas9-HF几乎没有可检测到的脱靶活性。
SaCas9基因组编辑应用程序的替代方法
“我们的这个新SaCas9的发展提供了对野生型Cas9工具箱,其中需要高度精确的基因组编辑的替代方案。这将是使用AAV载体在活体内递送基因组编辑‘药物’为将来的基因治疗特别有用,并且将与最新的“原始编辑” CRISPR平台兼容,该平台可以“搜索和替换”目标基因。”郑博士说。
